イギリスの「オックスフォード大学」と製薬会社「アストラゼネカ」が共同で行っているワクチン開発で良い結果が出ました。
この臨床試験は医学誌ランセットで発表された物で、1077人を対象にしたテストで9割の参加者からウイルス感染を防ぐ中和抗体反応が確認されたと報告されています。
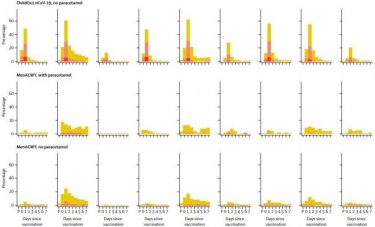
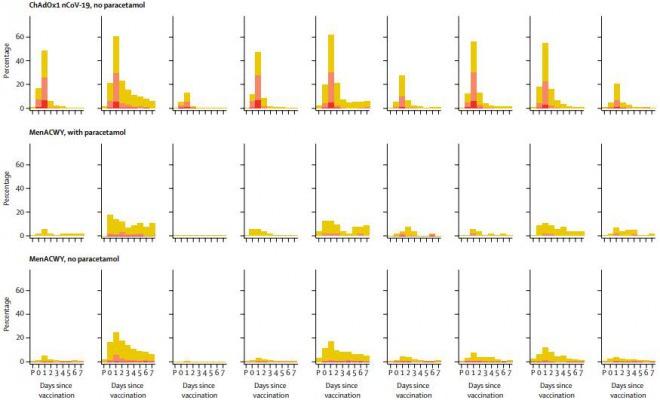
公開された報告書によると、1077人の参加者を「ワクチンを投与するグループ」と「ワクチンを投与しないグループ」に分けて反応を調査する形で行われ、新型コロナウイルスワクチンを投与したグループではT細胞による免疫反応が確認されたとのことです。
副作用に関しては「疲労感や頭痛の報告があっただけだ」とまとめられていました。
今回のワクチンはT細胞を活用するタイプのワクチンで、一般的なワクチンよりも長期に渡って抗体を維持することが出来るとされています。
新型コロナウイルスは2ヶ月程度で抗体の8割が消えると報告されているため、そこまで抗体が維持出来るかどうかが注目されているところです。
早ければ年内にも一部の人達を対象に投与を開始する見通しで、今後の報告に期待をしたいワクチンの一つだと言えます。
Background
The pandemic of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) might be curtailed by vaccination. We assessed the safety, reactogenicity, and immunogenicity of a viral vectored coronavirus vaccine that expresses the spike protein of SARS-CoV-2.
Methods
We did a phase 1/2, single-blind, randomised controlled trial in five trial sites in the UK of a chimpanzee adenovirus-vectored vaccine (ChAdOx1 nCoV-19) expressing the SARS-CoV-2 spike protein compared with a meningococcal conjugate vaccine (MenACWY) as control. Healthy adults aged 18–55 years with no history of laboratory confirmed SARS-CoV-2 infection or of COVID-19-like symptoms were randomly assigned (1:1) to receive ChAdOx1 nCoV-19 at a dose of 5 × 1010 viral particles or MenACWY as a single intramuscular injection. A protocol amendment in two of the five sites allowed prophylactic paracetamol to be administered before vaccination. Ten participants assigned to a non-randomised, unblinded ChAdOx1 nCoV-19 prime-boost group received a two-dose schedule, with the booster vaccine administered 28 days after the first dose. Humoral responses at baseline and following vaccination were assessed using a standardised total IgG ELISA against trimeric SARS-CoV-2 spike protein, a muliplexed immunoassay, three live SARS-CoV-2 neutralisation assays (a 50% plaque reduction neutralisation assay [PRNT50]; a microneutralisation assay [MNA50, MNA80, and MNA90]; and Marburg VN), and a pseudovirus neutralisation assay. Cellular responses were assessed using an ex-vivo interferon-γ enzyme-linked immunospot assay. The co-primary outcomes are to assess efficacy, as measured by cases of symptomatic virologically confirmed COVID-19, and safety, as measured by the occurrence of serious adverse events. Analyses were done by group allocation in participants who received the vaccine. Safety was assessed over 28 days after vaccination. Here, we report the preliminary findings on safety, reactogenicity, and cellular and humoral immune responses. The study is ongoing, and was registered at ISRCTN, 15281137, and ClinicalTrials.gov, NCT04324606.
オックスフォード大のワクチン、初期の治験で効果確認
https://www.asahi.com/articles/ASN7P2PPRN7PUHBI00B.html?twico
新型コロナウイルスのワクチンを開発しているオックスフォード大のチームが20日、人に投与する初期の臨床試験(治験)で安全性と免疫反応を起こす効果が確認されたと、英医学誌ランセットで発表した。病気から身を守る効果が十分かどうかを調べるには、より大規模な治験が必要だが、グループは「有望な結果だ」と期待している。
Just published @TheLancet, 2 trials of adenovirus-vectored vaccines against #SARSCoV2.
1) Safety and immunogenicity of the ChAdOx1 nCoV-19 vaccine against SARS-CoV-2: a preliminary report of a phase 1/2, single-blind, randomised controlled trial https://t.co/HKgPGKHu53 #COVID19— The Lancet Infectious Diseases (@TheLancetInfDis) July 20, 2020
英ワクチン、年内使用の可能性も https://t.co/Tk3TzxvwEk #tbs #tbs_news #japan #news
— TBS NEWS (@tbs_news) July 21, 2020
オックスフォード大のワクチン、初期の治験で効果確認https://t.co/egw5Jg8qhr
#新型コロナウイルス のワクチンを開発しているオックスフォード大のチームが、人に投与する初期の治験で安全性と免疫反応を起こす効果が確認されたと発表しました。 #英コロナワクチン— 朝日新聞デジタル編集部 (@asahicom) July 21, 2020
Safety and immunogenicity of the ChAdOx1 nCoV-19 vaccine against SARS-CoV-2: a preliminary report of a phase 1/2, single-blind, randomised controlled trial – The Lancet
まだ読んでないけどトレンド入りしてるワクチンの論文これっぽいですな
授業終わったら読む https://t.co/xWxRulmUeZ— にんにく (@ninnniku_g_poke) July 21, 2020
数時間前に一緒にメシ食うてた人と「いやぁワクチンは厳しいんとちゃいますか?数年レベルじゃないでしょ」と言うてたところに、まずまずencouragingな結果が。 https://t.co/zajaH6LijF
— 萩野 昇@平日は今日を含めてあと2日と思うとなんとか生きて行ける気がする (@Noboru_Hagino) July 20, 2020
待ち遠しいにもほどがある。。→オックスフォード大のワクチン、初期の治験で効果確認:朝日新聞デジタル https://t.co/0n26zWu1Aj #新型コロナウイルス
— 長野智子 (@nagano_t) July 21, 2020
英コロナワクチン、治験で好結果 アストラゼネカが共同開発:時事ドットコムhttps://t.co/SQ0oVCylaL
アストラゼネカのワクチンは英国や米国、ドイツ、フランスなどが供給契約を結んだほか、日本政府も確保に向けて同社と協議している。 https://t.co/VIjm3w8RLI— 足立康史 (@adachiyasushi) July 20, 2020

いいね!しよう